Nel contesto della medicina moderna e della gestione sanitaria sostenibile, la differenza tra farmaci generici e farmaci originali (o di marca) rappresenta un tema cruciale. Comprendere le caratteristiche, l'efficacia terapeutica, i processi produttivi e le implicazioni normative di queste due categorie di farmaci aiuta sia i professionisti sanitari che i pazienti a prendere decisioni informate.
Definizione: farmaco originale vs farmaco generico
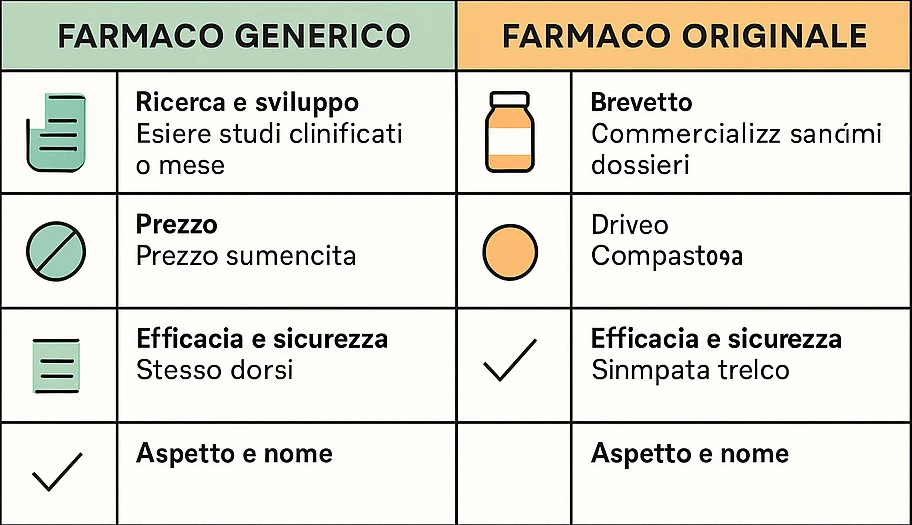
Farmaco originale: È il medicinale sviluppato e brevettato da un'azienda farmaceutica. La molecola attiva viene scoperta, testata clinicamente (fase I-III) e commercializzata dopo un lungo processo di ricerca e autorizzazione regolatoria. Dopo la sua immissione in commercio, l'azienda titolare gode di un'esclusiva commerciale per un periodo definito (in genere 20 anni dal deposito del brevetto).
Farmaco generico: È un medicinale che contiene lo stesso principio attivo del farmaco originale, nella stessa forma farmaceutica e dosaggio, ed è autorizzato a essere commercializzato dopo la scadenza del brevetto dell'originale. Deve dimostrare bioequivalenza, ossia la stessa efficacia e sicurezza terapeutica.
Efficacia e sicurezza: sono davvero equivalenti?
La principale preoccupazione tra i pazienti riguarda la presunta "minor efficacia" dei farmaci generici. Tuttavia, le autorità regolatorie come la FDA (Food and Drug Administration) e l'EMA (European Medicines Agency) richiedono studi rigorosi di bioequivalenza, che dimostrano che il generico raggiunge nel sangue concentrazioni simili al farmaco di riferimento.
Esempio pratico: Se un farmaco originale raggiunge una concentrazione massima (Cmax) di 100 ng/ml nel plasma, il generico approvato avrà una Cmax compresa tra l'80% e il 125% di quel valore, con variazioni clinicamente irrilevanti.
Inoltre, gli eccipienti possono differire, ma solo se non alterano l'efficacia, l'assorbimento o la tollerabilità del principio attivo.
Differenze nel costo e nell’accessibilità
Uno dei vantaggi principali dei farmaci generici è il costo inferiore, derivato principalmente dalla mancanza di spese per ricerca e sviluppo. Questo rende i generici più accessibili e rappresenta un risparmio notevole per i sistemi sanitari pubblici e privati.
Dati OMS: L’uso dei generici può ridurre la spesa farmaceutica di un paese fino al 70%, senza compromettere l’efficacia terapeutica.
Processo regolatorio: dalla sperimentazione all'autorizzazione
Mentre i farmaci originali richiedono:
- Ricerca preclinica su animali;
- Studi clinici in tre fasi su volontari e pazienti;
- Costi medi di sviluppo superiori ai 2 miliardi di dollari;
I farmaci generici:
- Saltano la sperimentazione clinica di fase II e III;
- Devono dimostrare bioequivalenza con studi clinici più brevi e meno costosi;
- Sono comunque sottoposti a GMP (Good Manufacturing Practices) e controlli post-marketing.
Perché alcuni medici e pazienti preferiscono ancora il farmaco originale?
Nonostante le evidenze scientifiche, alcune barriere culturali e psicologiche persistono:
- Effetto nocebo: la percezione che il generico sia meno efficace può ridurne l’effetto soggettivo;
- Brand trust: la fiducia consolidata in marchi noti influenza la preferenza;
- Formulazioni diverse: anche una lieve variazione negli eccipienti può influenzare la tollerabilità in pazienti sensibili (es. intolleranza al lattosio, allergie).
Il ruolo delle autorità regolatorie e della consulenza farmaceutica
Per garantire la qualità e la conformità dei farmaci generici con gli standard internazionali, aziende farmaceutiche e distributori si rivolgono a società di consulenza specializzate. Una di queste è statesideconsultants.com, che supporta le aziende nel:
- Navigare nel processo regolatorio presso FDA ed EMA;
- Preparare i dossier per l’ANDAs (Abbreviated New Drug Applications);
- Garantire la compliance normativa per l’immissione in commercio di generici in USA ed Europa;
- Supportare la strategia di lancio per ottimizzare tempistiche e accessibilità.
Grazie alla loro esperienza, enti come Stateside Consultants si rivelano essenziali nell’accelerare il processo di approvazione e nel minimizzare i rischi legati alla conformità normativa.
Conclusioni
I farmaci generici rappresentano una risorsa fondamentale per garantire l’accesso equo alla terapia farmacologica in tutto il mondo. Hanno la stessa efficacia, sicurezza e qualità dei farmaci originali, ma a un costo inferiore.